结合了诺贝尔获奖技术的新型超分辨显微镜
日前,由德国、阿根廷以及瑞典研究员共同开发了一款新型超分辨显微镜,结合了两项诺贝尔奖技术,在更高速率和更少发射光子条件下获得了纳米量级的超高分辨率。
传统光学显微镜的分辨率主要由瑞利标准进行限定:如果两个光学特征点在空间上的距离小于半个波长的距离时,衍射光的存在使得光斑界限变得模糊,特征点将无法区分。超分辨显微技术通过选择性地激发单个荧光分子,实现相邻的荧光分子的分辨,从而突破了瑞利标准的限制。

Stefan Hell(左)和他的同事们
凭借单分子显微技术,Eric Betzig和William Moerner获得了2014年的诺贝尔化学奖的。该技术通过随机的打开和关闭荧光分子,通过发射光子并利用其达到相机靶面上的位置来重建每个荧光分子的位置。但是,光子在传播时会发生衍射现象,导致对单个光子的位置产生不确定性。从同一个荧光分子采集多个光子可以降低这种不确定性,但想要获得单分子(纳米)的分辨率需要采集成千上万的光子。而且大多数荧光分子在发出如此数目的光子之前早已降解或漂白了。
环形光束
受激发射损耗(STED)显微术获得了2014诺贝尔化学奖的三分之一,此技术方案采用两个光束,第一个聚焦光束用来照射样品以打开荧光分子,第二个光束经过一个螺旋线状相位板调制,限定只有位于光圈中心的荧光物质可以激发出荧光及中心区域之外进行荧光抑制。通过在样品上进行光束共同扫描,可以准确定义发光分子的空间分布。然而这项技术的缺点是,为了在单分子光斑之外完全抑制荧光,环形光束能量将会破坏样品本身。因此,以上两种技术都难以获得单个分子的分辨率。
现在,诺贝尔奖得主Stefan Hell以及来自哥德廷马克斯普朗克生物物理化学研究所和其他几个研究所的科学家们开发出一种新型荧光显微镜,称为MINFLUX。他们在单分子显微镜中实现个别分子的随机开关,同时利用STED显微技术进行环形光束扫描以确定分子位置。
当光电探测器探测到信号时就意味着荧光分子的存在。由于光束呈现环形,其中心强度为零,距离越远强度越大。根据荧光分子的光强便可推算荧光分子距离光束焦点的距离。

具有纳米级的分辨率的锐化图像
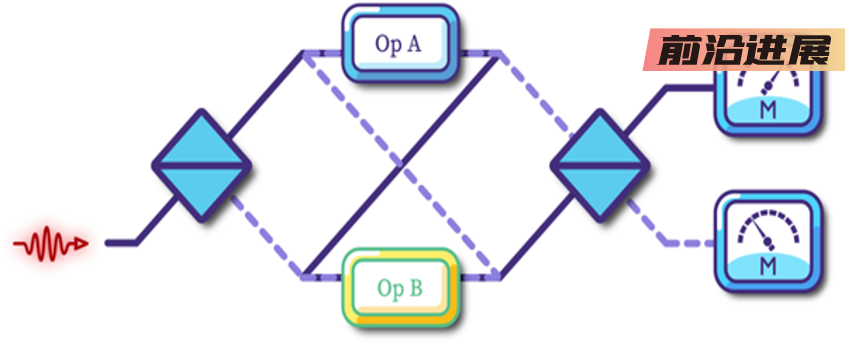
光束结构
通过光束瞄准荧光分子附近的四个点,并标记每个点的荧光强度,研究人员可以容易地计算出荧光分子距离每个点的距离,并由此推导出具有纳米级精度的位置。Hell解释说:“单分子显微镜中的坐标系由相机像素确定。而此系统由聚焦光束确定位置坐标系。”
研究人员通过MINFLUX系统来标记荧光分子的位置,能够映射得到具有特殊形状的DNA序列(DNA origamis),从而计算出它们的形状。在首次试验中,研究人员使用间隔11nm的荧光分子,只需50s的成像时间便可以发射并定位500个光子,平均空间不确定性为2.1nm。将荧光分子的空间间隔缩小到6nm,在120s内可以发射并接受1000个光子,测量的空间不确定缩小为1.2nm。
两倍的成像分辨率
MINFLUX的测量精度可以达到相同光子数单分子显微镜理论最大分辨率的两倍。此外,MINFLUX系统测量速度快,可以跟踪活体细菌内单个分子的运动。
单分子显微镜的发明者之一,美国哈佛大学的Xiaowei Zhuang表示:“通过采用高度创新的设计方法,MINFLUX绝对称得上一个真正意义上的突破。通过如此少量的光子可以达到超高精度的位置测量,这将极大有利于我们对细胞微观世界的探索。”
同样来自哈佛大学的Adam Cohen表示:“MINFLUX的设计方法巧妙,原理简单。近15年来,人们一直追寻不同应用层面的分子运动。在某些情况下,这种简单的设计理念将对我们的研究大有裨益。”同时,他也指出了在相对复杂细胞结构的应用中存在的潜在问题,“如果最先接收的光子并非来自目标分子,而是杂散光子,那么这些光子的追迹将会大大降低位置的测量精度。同时,随着样品中荧光分子数量的增多,对分子的开启和关闭也将越难保证。”