一种基于功能化修饰磁性纳米颗粒的石墨烯基光学生物传感器  下载: 1182次
下载: 1182次
1 引言
二维材料石墨烯具有很多独特的光电特性,研究发现,在全内反射条件下,利用石墨烯的偏振选择吸收特性[1-2],可构建出一种高折射率灵敏度的石墨烯基生物传感器[3]。同现有的基于表面等离子激元(SPR)的传感技术相比[4-5],石墨烯基的光学生物传感器具有灵敏度高、纵向探测深度大和结构简单等优点。在细胞检测、免疫识别和药物敏感性等领域具有广阔的应用前景[6-9]。
利用折射率敏感的生物传感器进行特异性生物小分子检测具有重要的应用价值。传统的SPR生物传感器可以在金膜表面直接修饰生物探针,且这种制备工艺已相对成熟。文献[ 10]中利用SPR传感器的金膜表面巯基(—SH)直接与适配体(aptamer)形成共价键结构,成功地实现了赭曲毒素A(OTA)的检测。文献[ 11]中采用SPR生物传感器对山羊IgMt抗体进行检测,检测过程中同样采用金膜表面巯基(—SH)直接与适配体形成共价键的连接方式。然而对于石墨烯基的生物传感器,不同实验室制备的石墨烯参差不齐,不同方式合成的石墨烯表面带有不同的官能团,修饰方法各异,如:采用石墨烯基光学传感器检测兔IgG蛋白时,需对氧化还原石墨烯功能团进行活化处理,然后再与适配体连接[8];利用石墨烯基光学传感器对特定气体NO2检测时,需要对石墨烯表面进行特殊的磺基化处理后才能进行特异性检测[12]。Fe3O4基磁性纳米颗粒经常被用于分离纯化大分子试剂、药物递送载体等[13],由于Au具有较好的生物相容性能,且易与巯基结合,因此带有Au核壳结构的Fe3O4基复合纳米颗粒常被用于修饰生物分子,通过外界磁场的控制,可实现快速生物分子的递送[14-17],如Guo[18]将Fe3O4@Au磁性纳米颗粒用于SPR传感系统中,实现了样品分子至金膜表面的快速吸附。
本文给出了一种于功能化修饰磁性纳米颗粒的石墨烯基光学生物传感器,在全内反射条件下,将修饰有生物探针磁性纳米颗粒,通过磁场控制吸附在石墨烯基的传感器表面,基于石墨烯偏振选择吸收特性,实现高灵敏度、特异性的生物小分子的实时检测,替代了在石墨烯表面直接修饰生物探针的复杂过程。研究发现,吸附的磁性纳米颗粒相比于传统SPR传感器的金膜表面具有更大的表面积,由于石墨烯基光学生物传感器的纵向探测深度较大[3,6-7,10,19-22],故可进一步提高传感灵敏度,使其更加适用于低浓度生物小分子的检测。利用上述方法对小浓度的OTA的检测结果表明,实现了动态范围0.01~5 ng·mL-1的 OTA实时检测。
2 基于功能化修饰磁性颗粒的折射率传感
2.1 石墨烯偏振选择吸收特性
石墨烯具有独特的电子结构,其导带和价带在狄拉克点相遇,因此本征石墨烯在不同频率的入射光波激发时具有固定的电导率。多层石墨烯可看作单层石墨烯的动态叠加,则N层石墨烯的介电常数
式中:σg为单层石墨烯的介电常数;N为石墨烯的层数。研究表明,当光波波长为532 nm时,可以计算出单层石墨烯的动态介电常数为σg=60.853-0.078i[20]。
基于石墨烯偏振选择吸收特性,构建全内反射(TIR)条件下含有石墨烯的三明治结构模型,示意图如
式中:μ0为真空磁导率;γ为真空电导率;θ1、θ2分别为光由光密介质入射到光疏介质的入射角和折射角;n1和n2分别为光密介质和光疏介质的折射率。本研究采用光密介质为BK7玻璃(n1=1.517),光疏介质为水(n2=1.333)。因为单层石墨烯的厚度仅为0.34 nm,所以在计算过程中其厚度相对于周围的电介质可以忽略。
同理,对于TM偏振模式下的电磁波,反射率rp、透射率tp和吸收率αp可表示为
基于上述模型可以测量光疏介质的折射率变化,实验中采用的入射光的波长为532 nm,采用化学沉积法(CVD)制备的石墨烯(层数N=10)。理论模拟得到入射光为不同偏振态时的反射率与入射角的关系曲线,如
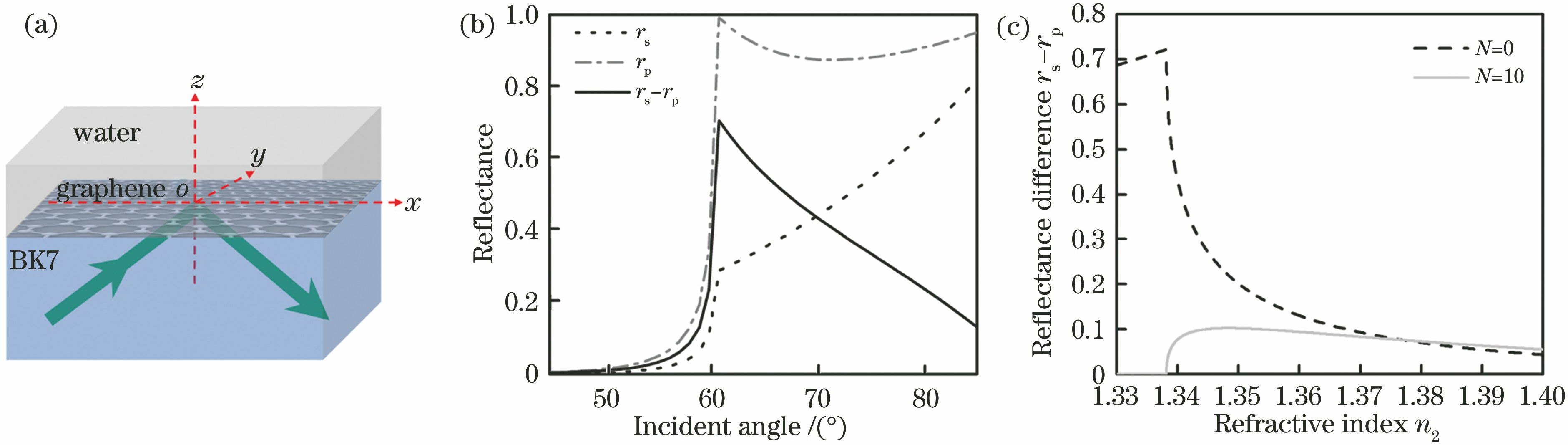
图 1. TIR条件下的石墨烯偏振选择吸收特性。(a) TIR条件下含有石墨烯的三明治结构模型;(b) TIR条件下含有石墨烯时不同偏振态反射率与入射角的关系;(c)有无石墨烯两种情况下反射率差值与光疏介质折射率的关系
Fig. 1. Polarization-sensitive absorption of graphene under TIR condition. (a) Sandwich structure model with graphene under TIR condition; (b) relationship between the reflectance at TE/TM polarization states and the incident angle with graphene under TIR condition; (c) relationship between the reflectance difference and the refractive index of the optically thinner medium with/without graphene
2.2 石墨烯基的光学生物传感器
基于上述原理搭建了石墨烯的光学生物传感器,其原理如
利用上述折射率传感器可在分子水平实现特异性生物小分子的高灵敏检测。为了克服直接在石墨烯表面直接修饰生物探针的技术手段不成熟的问题,本研究采用Au纳米颗粒包裹四氧化三铁磁性颗粒(Fe3O4@Au)作为生物探针载体,其表面的Au具有较好的生物相容性,常用于修饰生物分子。测量流程如
2.3 纳米磁性颗粒的功能化修饰
Fe3O4@Au纳米颗粒(100 nm)的制备是由Fe3O4磁性纳米颗粒(70 nm)修饰聚吡咯,再由Au纳米颗粒(5 nm)包覆[24],其电镜显微图(TEM)如

图 3. 功能化修饰的磁性纳米颗粒的折射率传感流程图
Fig. 3. Flowchart of refractive index sensing for functionalized magnetic nanoparticles

图 4. Fe3O4@Au磁性纳米颗粒的修饰。(a) Fe3O4@Au纳米颗粒的TEM图;(b) Fe3O4@Au纳米颗粒的紫外可见光谱
Fig. 4. Modification of Fe3O4@Au magnetic nanoparticles. (a) TEM image of Fe3O4@Au nanoparticles; (b) UV-visible spectrum of Fe3O4@Au nanoparticles
3 实验结果与分析
3.1 折射率传感特性分析
首先对搭建的石墨烯基光学生物传感器实验平台的传感特性进行测量,配制了质量分数分别为0%、0.005%、0.01%、0.05%、0.1%、0.5%、1%的氯化钠溶液,溶剂为去离子水,氯化钠溶液的质量分数与折射率满足
式中:nNaCl为氯化钠溶液的折射率;nwater为去离子水的折射率;c为氯化钠溶液的质量分数。
该生物传感器的灵敏度S(n)可以表示为
式中:Δu为电压变化值;Δn为微小折射率。实验中采用配制不同浓度的氯化钠溶液来实现折射率的微小变化。
分辨率R可以表示为
式中:σ为多次采样计算得到的标准差。
将不同质量分数的氯化钠溶液依次分别通入微流腔中,得到实时电压信号与氯化钠溶液折射率的关系如

图 5. 不同浓度氯化钠溶液对应折射率的电压响应。(a)实时电压变化;(b)折射率与电压关系
Fig. 5. Voltage response of refractive index at different sodium chloride concentrations. (a) Real-time voltage change; (b) relationship of refractive index and voltage
3.2 Fe3O4@Au-aptamer磁性纳米颗粒的吸附
在石墨烯基的光学生物芯片的微流腔中,注入质量浓度为1 mg/mL的Fe3O4@Au-aptamer磁性颗粒悬浮液,首先在不加入磁铁时,静置22 min,测量传感器输出电压值随时间的变化,其结果如

图 6. 磁性纳米颗粒固定的实时电压响应
Fig. 6. Real-time voltage response when magnetic nanoparticles was immobilized on the surface of graphene

图 7. 不同磁场强度下磁性颗粒吸附在石墨烯表面的明场显微图像。(a) 0 mT; (b) 80 mT
Fig. 7. Bright-field micrograph of magnetic nanoparticles adsorbed on the surface of graphene under different magnetic field intensities. (a) 0 mT; (b) 80 mT
3.3 OTA的检测
为了验证所提方法的有效性,对小浓度的OTA进行检测。OTA是一种对人体健康有害且分子量只有403 g/mol的生物小分子,由于其广泛存在于各种作物和食品中,故实现其高灵敏检测尤为重要[25-26]。本研究配制质量浓度分别为0.01、0.5、1、2、5 ng·mL-1的OTA溶液,采用磷酸盐缓冲液作为溶剂。在微流腔内充入修饰有适配体DNA的Fe3O4@Au-aptamer磁性颗粒,在磁场作用下将其吸附在石墨烯传感表面。分别将不同浓度的OTA样品以20 μL·min-1的速度注入微流腔中,测量传感器输出电压值随响应时间的变化,实验结果如
为了验证修饰有适配体DNA的Fe3O4@Au-aptamer磁性颗粒的特异性,采用黄曲霉毒素B1(Aflatoxin B1,AFB1)在相同条件下进行了对照实验。在微流腔内分别充入质量浓度为0.01 ng·mL-1和2 ng·mL-1的AFB1样品,测量传感器输出电压值,并将其与充入同样浓度OTA样品时的输出电压值进行比较,实验结果如

图 8. 不同浓度OTA实时电压响应
Fig. 8. Real-time voltage response of Ochratoxin A at different concentrations

图 9. 不同浓度OTA与传感器输出电压的关系
Fig. 9. Relationship between different concentrations of Ochratoxin A and output voltage

图 10. AFB1与OTA电压响应的比较
Fig. 10. Comparison of voltage response of aflatoxin B1 and ochratoxin A
4 结论
研究表明,采用生物相容性好的Fe3O4@Au纳米复合材料作为探针适配体的载体,通过控制磁场使其吸附在石墨烯传感器表面,有效地克服了直接在石墨烯表面修饰生物探针困难的问题,扩展了石墨烯基的光学生物传感器的应用范围。利用自行搭建的基于功能化修饰磁性颗粒的石墨烯基光学生物传感器,实现了0.01 ng·mL-1的超低浓度OTA分子的检测,且在0.01~5 ng·mL-1浓度范围内具有良好的响应。与AFB1样品对照实验表明,在磁性颗粒表面修饰的OTA适配体探针具有较好的特异性。本文所提出的基于功能化修饰磁性颗粒的石墨烯基光学生物传感器,作为一种实现特异性生物小分子的高灵敏检测方法,具有一定的普适性,不仅可实现本文给出的低浓度OTA的检测,还可以通过改变适配体核苷酸的顺序,实现其他毒素小分子的特异性高灵敏检测,其在食品安全、药物开发与筛选、细胞检测、免疫识别和遗传分析等领域具有广阔的应用前景。
[1] Bao Q L, Zhang H, Wang B, et al. Broadband graphene polarizer[J]. Nature Photonics, 2011, 5(7): 411-415.
[2] Ye Q, Wang J, Liu Z B, et al. Polarization-dependent optical absorption of graphene under total internal reflection[J]. Applied Physics Letters, 2013, 102(2): 021912.
[3] Xing F, Liu Z B, Deng Z C, et al. Sensitive real-time monitoring of refractive indexes using a novel graphene-based optical sensor[J]. Scientific Reports, 2012, 2: 908.
[4] Peterson A W, Halter M, Tona A, et al. High resolution surface plasmon resonance imaging for single cells[J]. BMC Cell Biology, 2014, 15: 35.
[5] 陈强华, 刘景海, 罗会甫, 等. 一种基于表面等离子共振的液体折射率测量系统[J]. 光学学报, 2015, 35(5): 0512002.
[6] Sun L X, Zhang Y Q, Wang Y J, et al. Real-time subcellular imaging based on graphene biosensors[J]. Nanoscale, 2018, 10(4): 1759-1765.
[7] Wang Y J, Zhang S W, Xu T, et al. Ultra-sensitive and ultra-fast detection of whole unlabeled living cancer cell responses to paclitaxel with a graphene-based biosensor[J]. Sensors and Actuators B: Chemical, 2018, 263: 417-425.
[8] Jiang W S, Xin W, Xun S, et al. Reduced graphene oxide-based optical sensor for detecting specific protein[J]. Sensors and Actuators B: Chemical, 2017, 249: 142-148.
[9] 刘璐, 吴晓静, 孙伽略, 等. 大穿透深度折射率传感器对活细胞药物敏感性的研究[J]. 光学学报, 2018, 38(11): 1104001.
[10] Bianco M. Sonato A, de Girolamo A, et al. An aptamer-based SPR-polarization platform for high sensitive OTA detection[J]. Sensors and Actuators B: Chemical, 2017, 241: 314-320.
[11] Zhang H, Sun Y, Wang J, et al. Preparation and application of novel nanocomposites of magnetic-Au nanorod in SPR biosensor[J]. Biosensors and Bioelectronics, 2012, 34(1): 137-143.
[12] Xing F, Zhang S, Yang Y, et al. Chemically modified graphene films for high-performance optical NO2 sensors[J]. The Analyst, 2016, 141(15): 4725-4732.
[14] Miao P, Tang Y G, Wang L. DNA modified Fe3O4@Au magnetic nanoparticles as selective probes for simultaneous detection of heavy metal ions[J]. ACS Applied Materials & Interfaces, 2017, 9(4): 3940-3947.
[15] Chen H X, Qi F J, Zhou H J, et al. Fe3O4@Au nanoparticles as a means of signal enhancement in surface plasmon resonance spectroscopy for thrombin detection[J]. Sensors and Actuators B: Chemical, 2015, 212: 505-511.
[17] 李春梅. 金纳米与磁纳米颗粒及其复合物的生物传感和细胞成像研究[D]. 重庆: 西南大学, 2013: 69- 87.
Li CM. Applications of AuNPs, Fe3O4 Nanoparticles and Fe3O4@Au nanorose in biosensing and cell imaging[D]. Chongqing: Southwest University, 2013: 69- 87.
[18] Guo X W. Fe3O4@Au nanoparticles enhanced surface plasmon resonance for ultrasensitive immunoassay[J]. Sensors and Actuators B: Chemical, 2014, 205: 276-280.
[19] Sun L X, Zhang Y Q, Wang Y J, et al. Refractive index mapping of single cells with a graphene-based optical sensor[J]. Sensors and Actuators B: Chemical, 2017, 242: 41-46.
[20] Sun L X, Zhang Y Q, Zhang C L, et al. Refractive index sensing and imaging based on polarization-sensitive graphene[J]. Optics Express, 2019, 27(20): 29273-29286.
[22] Yang Y, Sun J L, Liu L, et al. Research of detection depth for graphene-based optical sensor[J]. Optics Communications, 2018, 411: 143-147.
[23] Chikazawa J I, Uwada T, Furube A, et al. Flow-induced transport via optical heating of a single gold nanoparticle[J]. The Journal of Physical Chemistry C, 2019, 123(7): 4512-4522.
[24] Zhang H, Zhong X, Xu J J, et al. Fe3O4/polypyrrole/Au nanocomposites with core/shell/shell structure: synthesis, characterization, and their electrochemical properties[J]. Langmuir, 2008, 24(23): 13748-13752.
[25] Meulenberg E P. Immunochemical methods for ochratoxin A detection: a review[J]. Toxins, 2012, 4(4): 244-266.
[26] Mateo R, Medina Á, Mateo E M, et al. An overview of ochratoxin A in beer and wine[J]. International Journal of Food Microbiology, 2007, 119(1/2): 79-83.
[27] Al Rubaye A, Nabok A, Catanante G, et al. Detection of ochratoxin A in aptamer assay using total internal reflection ellipsometry[J]. Sensors and Actuators B: Chemical, 2018, 263: 248-251.
Article Outline
张慧琴, 孙立勋, 杨艺哲, 吴晓静, 杨勇, 朱思伟, 袁小聪. 一种基于功能化修饰磁性纳米颗粒的石墨烯基光学生物传感器[J]. 光学学报, 2020, 40(11): 1117001. Huiqin Zhang, Lixun Sun, Yizhe Yang, Xiaojing Wu, Yong Yang, Siwei Zhu, Xiaocong Yuan. Graphene-Based Optical Biosensor Using Functionalized Magnetic Nanoparticles[J]. Acta Optica Sinica, 2020, 40(11): 1117001.







